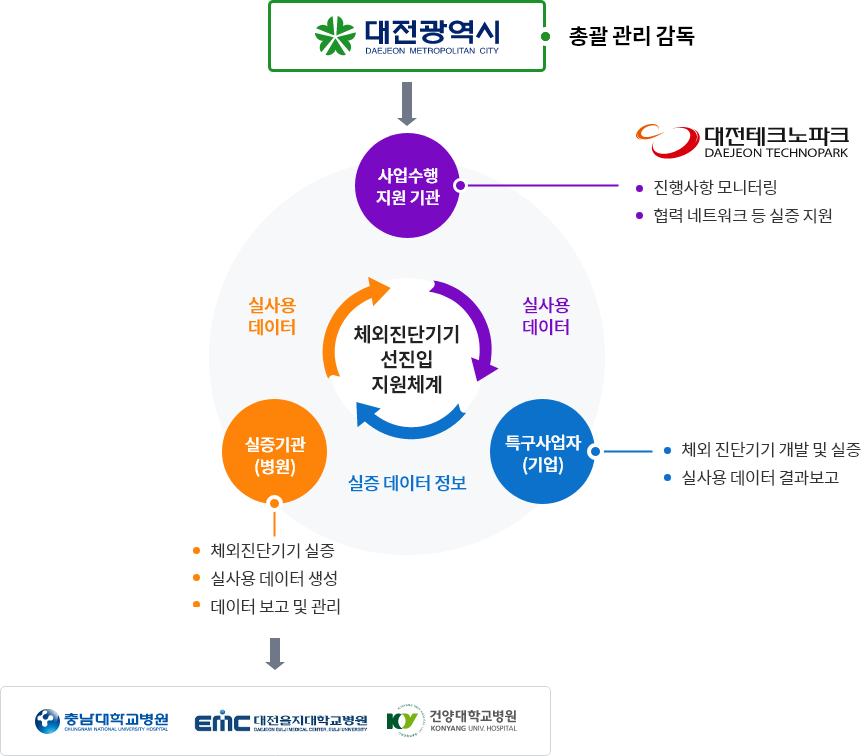
사업내용
![]()
- 신의료기술을 활용한 체외진단기기는 식약처 인·허가 및 신의료기술평가 등 절차에 따른 시장진출 지체
![]()
- 실증데이터 수집관련 관리감독(모니터링)을 실시하기 위한 관리감독기구를 운영하고 실사용 의료데이터의 확보 및 수집지원을 위한 실증기관(병원)연계
![]()
-
기업㈜이앤에스헬스케어, ㈜싸이토딕스,
㈜파나진, ㈜시선바이오머티리얼스,
㈜수젠텍, ㈜딥바이오, ㈜솔젠트,
㈜레보스케치, ㈜바이오니아,
㈜프로테옴텍 - 병원충남대학교병원, 대전을지대학교병원, 건양대학교병원
- TP대전테크노파크
규제특례에 관한 사항
체외진단기기 신의료 평가 유예기간 연장(1→2년)
신의료기술평가유예 절차 간소화 실증
※ 신의료기술평가에 관한 규칙 제2조 및 제3조체외진단기기의 신의료기술 평가 유예 절차 간소화 실증
-
사업자
대전테크노파크, 충남대병원, 을지대병원, 건양대병원, ㈜딥바이오 등 10개사
- 세부사업 정의
체외진단기기 신의료 평가 유예기간 연장(1→2년) 신의료기술평가유예 신청시 제출서류면제- (대상질환) 만성 중증질환(암 등), 치매
- (실시기관) 을지대병원, 충남대병원, 건양대병원
- (모니터링) 대전시는 진행사항 모니터링 결과를 분기별로 복지부와 한국보건의료연구원에 공유
- 규제특례 등
실증특례- 신의료기술평가에 관한 규칙 제2조 및 제3조
- 세부사업 정의
실증특례 체외진단기기의 신의료기술 평가유예 절차 간소화 실증
체외진단기기의 신의료기술 평가 유예기간 연장 실증 (1 -> 2년) 체외진단검사분야 신의료기술 평가유예 신청 시 제출 서류 간소화
바이오메디컬 규제자유특구 실증 세부내용 2